en una fractura expuesta se corre el peligro de
miércoles, 27 de octubre de 2010
Materiales de Osteosintesis
Materiales de Osteosintesis
Introducción

Se necesitaba pues de técnicas y sistemas específicos para el territorio maxilofacial dadas sus peculiaridades anatómicas, fisiológicas y biomecánicas, con un doble objetivo: la reparación anatómica con restauración funcional lo más precoz posible y una disminución drástica de la morbilidad.
Osteosíntesis y biomateriales
Diferentes estudios experimentales en el campo de la biomecánica y fisiopatología de la consolidación ósea así como la investigación y perfeccionamiento de los biomateriales empleados, han resultado en los últimos 25 años en un vertiginoso avance en cuanto a técnicas y sistemas, gracias a los cuales se ha producido una considerable disminución en los índices de complicaciones y fracasos terapéuticos en el manejo de las diferentes técnicas de osteosíntesis craneofacial.

A toda placa de osteosíntesis se le exigen unas propiedades mínimas, fundamentalmente resistencia adecuada (para proporcionar estabilidad), ductilidad suficiente (para permitir un moldeado anatómico) y biocompatibilidad (para no producir efectos adversos locales o sistémicos). Los materiales con los que se fabrican los implantes para osteosíntesis son variados; se usan principalmente acero inoxidable, aleaciones de cobalto-cromo-molibdeno y el titanio, puro o aleado. Durante muchos años, el acero inoxidable fue el material de elección. Consiste en una aleación de los metales hierro, cromo, níquel y molibdeno en proporciones bien definidas (62,5-17,5-14,5 y 2,8% respectivamente) asociados a otros componentes en menor proporción. Su resistencia, compatibilidad y propiedades anticorrosivas (ligadas proporcionalmente a la presencia de cromo) resultan adecuadas, aunque en 1977 Steinemann describe cierta potencialidad autocorrosiva por interacción entre diferentes componentes metálicos del implante fretting corrosion. Esta circunstancia aconseja la sistemática retirada de materiales de acero inoxidable una vez consolidada y mineralizada la fractura, al año aproximadamente de la intervención.
En este desarrollo tecnológico al que hacíamos referencia, el titanio como biomaterial se ha convertido en uno de los protagonistas indiscutibles, dada su extremada pasividad química (y por tanto excelente biocompatibilidad) y por reunir las propiedades físicas adecuadas para un buen comportamiento biomecánico a largo plazo. Su densidad hace que los implantes pesen alrededor de un 45% menos que los implantes de acero y de cobalto, factor importante respecto a la comodidad del paciente sobre todo en fijaciones largas. Su bajo módulo de elasticidad es otra ventaja, ya que minimiza la protección contra la presión y ésta se transfiere al hueso; la relativa importancia de la protección contra la presión se incrementa a medida que aumenta el tamaño del implante. Por todo ello, desde mediados de los 80 los implantes fabricados con titanio puro son de elección para la osteosíntesis en el territorio cráneomaxilofacial.

El titanio
El titanio (Ti) fue descubierto en 1791, asignándosele el nº 22 en la Tabla Periódica de Elementos, y constituye el noveno elemento en abundancia de la corteza terrestre, encontrándose en concentraciones significativas sobre todo en mena de rutilo (en forma de TiO2) y en ilmenita (FeO.TiO2). En la actualidad, su «síntesis» como metal puro se realiza a partir de estos minerales mediante la técnica desarrollada por Kroll en 1937: reducción del tetracloruro de titanio con magnesio en atmósfera de argón para evitar su oxidación.
A mediados de los años 50, los estudios relativos al titanio y sus aleaciones sufrieron un gran impulso, fundamentalmente en EE.UU., dada la gran importancia que sus propiedades físico-químicas le conferían en el desarrollo de tecnología militar y aerospacial sobre todo: baja densidad, bajo módulo de elasticidad, excelente relación resistencia mecánica / densidad, buen comportamiento a altas temperaturas, gran resistencia a la corrosión y magnifica biocompatibilidad. En la siguiente década, sus aplicaciones fueron ampliadas a la industria química y biomédica.


El titanio es considerado como un metal ligero, el único que presenta dimorfismo; en estado puro su microestructura cristalina y estable es hexagonal, pasando a ser cúbica e inestable a partir de 882°C (tª de tránsito). Esta transformación permite realizar combinaciones con diferentes elementos y, consecuentemente, obtener aleaciones con diferentes estructuras cristalográficas y por tanto propiedades físico-químicas. Distinguimos tres tipos:
• Aleaciones a son las que presentan una estructura hexagonal a temperatura ambiente, y en ellas el efecto del aleante consiste en aumentar la temperatura de tránsito. El titanio comercialmente puro pertenece a este grupo.
• Aleaciones b son las que presentan una estructura cúbica a temperatura ambiente, y en ellas el efecto del aleante es precisamente hacer estable esta microestructura a esta temperatura.
• En las aleaciones a/b la microestructura es mixta (globular) y estable; el TAV (aleación de Titanio/6% Aluminio/4% Vanadio) pertenece a este grupo.
El titanio «comercialmente puro» (Ti CP) es simplemente titanio y oxígeno, junto a otras «impurezas». En efecto, el titanio metálico puro reacciona muy rápidamente con el oxígeno, nitrógeno, hidrógeno y carbono de la atmósfera, por lo que en su obtención para fines comerciales presenta estas impurezas en su composición en diferentes proporciones, lo que da lugar hasta a cuatro tipos de combinaciones con diferentes grados de resistencia y ductilidad (Grados 1 a 4 de la Norma ASTM F67)
El TAN (Titanio/6% Aluminio/7% Niobio) es una aleación relativamente nueva seleccionada por la AO/ASIF para las futuras generaciones de implantes diseñados para la fijación de fracturas. La aleación fue concebida en 1977 por un equipo de investigadores en Sulzer Bros (Winterthur-Suiza) e introducida en 1985 en la práctica clínica (prótesis de reemplazo total de cadera). Las propiedades mecánicas de la aleación TAN son muy similares a la aleación Ti-6Al-4V, utilizada como biomaterial desde hace años. Se ha sustituido el Vanadio por Niobio, metal descubierto por Hatchett en Connecticut en 1801 e inicialmente denominado Columbio, asignándosele el nº 41 en la Tabla Periódica de Elementos.

Su composición queda recogida en la tabla 3, siendo trascendental que los contenidos en hidrógeno sean mínimos para evitar la fractura de la aleación. Su microestructura es mixta a/b globular, muy similar al TAV, por lo que sus propiedades físicas son también muy parecidas (densidad, módulo de elasticidad, sensibilidad a la tensión, fatiga rotacional, corrosión, etc.). Con respecto al Ti CP Grado 4, posee sustanciales ventajas, que podríamos resumir a efectos prácticos en una mejor relación del binomio manejabilidad/ resistencia. Desde el punto de vista de labiocompatibilidad el TAN sigue el principio de utilizar solamente elementos no tóxicos para implantes indicado en la patente USA 4,029,129 asignada al Instituto Straumann (Waldenburg- Suiza).

Numerosos estudios experimentales in vivo e in vitro sustentan la excelente biocompatibilidad de esta aleación y ciertas ventajas (al menos en el campo teórico y experimental) con respecto a los compuestos con Vanadio. Finalmente, el análisis espectroscópico de fotoelectrones ha determinado que la superficie del TAN es una capa mixta de óxido de titanio, óxido de aluminio y óxido de niobio, más estable químicamente que las capas de óxido de titanio formadas en el Ti CP, por lo que la resistencia a la corrosión es si cabe mayor. Tratamientos de superficie como el anonizado de los implantes permiten determinar el espesor de esta capa de óxido mixta, que es el que condiciona el color que presentan los implantes por difracción de la luz en el interior del óxido (típicamente dorado en los implantes AO).
Un ejemplo de estos implantes de última generación lo constituyen en nuestro territorio los tornillos de fijación para los sistemas de bloqueo tipo UNILOCK 2.0.
Osteosíntesis y radioterapia
En la actualidad, la osteosíntesis mandibular con placas de titanio tras procedimientos ablativos oncológicos es una técnica rutinaria y perfectamente sistematizada. Usualmente son utilizadas técnicas de fijación en osteotomías de abordaje, para el refuerzo en madibulectomías marginales, en el puenteo de defectos óseos tras mandibulectomías segmentarias y en la fijación de injertos óseos microvascularizados o libres. Según el caso, distintos tipos de fijaciones son empleados, y en su elección, la presencia de radioterapia pre o postoperatoria es un factor determinante. Como norma general, deberá procurarse una fijación rígida, suficientemente estable, sobre aquellas áreas radiadas o que quedarán incluidas en campos de radiación.
Es bien conocido que la radioterapia condiciona un aumento en el índice de complicaciones locales, incluyendo entre otras fracasos de las osteosíntesis. Sin embargo, no está sólidamente establecida en la bibliografía una relación causal directa y significativa entre la presencia de material de osteosíntesis y la aparición de estas complicaciones, siendo su génesis multifactorial.
Diversos factores locales han sido establecidos como responsables de este fenómeno, entre los que destacan la localización anatómica del defecto mandibular y la presencia o no de una cobertura adecuada de los implantes con colgajos vascularizados. Típicamente, las complicaciones son más frecuentes en ausencia de esta cobertura y en las regiones sinfisaria y del cuerpo mandibular, justo por delante del «estuche» maseterino. Los factores tisulares relacionados con este incremento en la morbilidad son fundamentalmente las alteraciones que la radioterapia ocasiona en la microvascularización ósea y de los tejidos conectivos, que condicionan un retraso en el proceso de cicatrización y regeneración tisular. Finalmente, también se han establecido efectos deletéreos de tipo bioquímico como los que se producen sobre la actividad de la BMP (proteína ósea morfogenética). Consecuentemente, la consolidación de una osteotomía y el proceso de osteointegración entre tornillos y hueso se ven enlentecidos con un aumento en las posibilidades de fracaso, máxime si consideramos que por los mismos motivos locales y tisulares, el riesgo de infección también está incrementado. En estas circunstancias, el empleo de una fijación no suficientemente estable casi garantiza la presentación de complicaciones.
Un segundo aspecto a considerar es la interacción que se produce entre el metal de los implantes y la radiación. Es bien conocido que la distribución de la dosis resulta alterada, produciéndose un incremento de la misma debido a un fenómeno de dispersión por delante del implante y una atenuación por un efecto de absorción distalmente al mismo. Desde el punto de vista experimental, ha quedado establecido que estos cambios son directamente proporcionales al nº atómico del metal interpuesto y a los «perfiles» (en términos de grosor y anchura) del implante, quedando limitados a un área entre 1-5 mm alrededor de la placa, con una media dosimétrica de menos del 3% para el fenómeno de dispersión a los 2 mm y del 4% para el fenómeno de absorción a los 5 mm. Estas variaciones quedan sin embargo «compensadas» cuando se utilizan campos paralelos y opuestos (Ryu-1995). En la práctica clínica, estos fenómenos pudieran tener dos repercusiones importantes: sobre el control oncológico, por atenuación e infradosis, y sobre la radionecrosis tisular por sobredosis.
En el primer caso, y con los datos de que se disponen, parece poco probable que tras la realización de una cirugía oncológica ad hoc con márgenes oncológicos macroscópicos de seguridad y con el eventual empleo de colgajos reconstructivos, la interposición de una placa pudiera interferir sobre la dosis terapéutica que el lecho quirúrgico tumoral hubiese de recibir; no hay evidencia científica de un incremento en la tasa de recidivas locales por este motivo.
En el segundo aspecto, la dispersión sí pudiera tener repercusión clínica, ya que puede producirse más probablemente una osteoradionecrosis focal por sobredosis en la interfase hueso-tornillo, con el consiguiente fracaso del sistema de osteosíntesis aplicado, o una mayor radionecrosis tisular, mucosa o cutánea, con mayor riesgo de exposición de placa intra o extraoral.
En resumen, y dado que la radioterapia de cabeza y cuello usualmente utiliza campos paralelos y opuestos, las variaciones en la dosis terapéutica por dispersión y absorción se compensan sin tener una repercusión significativa en el control oncológico local e incluso, para la mayoría de los autores, en los fenómenos de radionecrosis focal. En cualquier caso, y en función de su nº atómico, las aleaciones de titanio son también en este aspecto menos interactivas y, por lo tanto, de elección en presencia de radioterapia adyuvante respecto a las de acero.
En la práctica clínica, la opción de una Placa de Bloqueo (tipo UNILOCK) sería electiva en todos los casos en los que deba coexistir con la radioterapia, no ya por sus más bajos perfiles sino, sobretodo, por minimizarse al máximo la isquemia que sobre la cortical ósea provoca la compresión de una placa tradicional.
Finalmente, cabe insistir en que los índices de complicaciones y fracasos achacados al binomio Radioterapia / Osteosíntesis se minimizan en presencia de una cobertura tisular adecuada y mediante la restauración anatómica con injertos óseos microvascularizados de los defectos mandibulares. La opción de la osteosíntesis puente, con el implante adecuado, debería reservarse para defectos muy posteriores o para pacientes con un pronóstico oncológico muy desfavorable.
Retirada de osteosíntesis
Una vez consolidada la fractura u osteotomía los materiales de osteosíntesis pierden su efecto biomecánico de fijación interfragmentaria y se convierten en cuerpos mecánicamente inertes. El hueso subyacente se remodela de forma reactiva al stress vascular que le supone el tener adosada la placa. Este proceso ocurre en los primeros meses del postoperatorio y cursa con una fase inicial de cierta porosis que queda resuelta si la circulación intracortical está indemne, circunstancia que se da cuando la técnica de osteosíntesis ha sido adecuada. En ocasiones, transcurrido el tiempo necesario, el grado de osteointegración es tal que se produce neoformación ósea sobre la placa de osteosíntesis (Fig. 9). En esta situación, transcurrido un año de la cirugía, la decisión de proceder a la retirada del material de osteosíntesis, caso de haber utilizado titanio, resulta comprometida. Supone una nueva intervención quirúrgica, a menudo con anestesia general, no exenta de ciertos riesgos locales y sistémicos. Además, en muchas ocasiones la osteointegración es tal que hay que realizar ostectomías para poder retirar el material, los tornillos pueden descabezarse permaneciendo el vástago en el espesor del hueso, etc. En definitiva, puede darse una situación de agresión local desmesurada, con riesgo de complicaciones, que debe estar justificada. No podemos obviar que en muchas ocasiones, y en algunos países más que en otros, la sistemática retirada de las osteosíntesis obedece más a criterios socio-sanitarios y económicos que a los estrictamente biomédicos.

Las principales indicaciones, casi siempre relativas, para proceder a retirar los materiales de fijación serian:
• Intolerancia al frío.
• Palpación subcutánea y sensibilidad.
• Exposición intra-extraoral.
• Interferencia con prótesis.
• Interferencia con implantes dentales.
• Inestabilidad. Movilidad de la placa y/o aflojamiento de los tornillos, por infección y/o por error técnico.
• Reacciones adversas (tóxicas) locales ó generales: hardware de acero inoxidable.
Otra posible desventaja (invocada en la literatura) que podría justificar bien la retirada de material de osteosíntesis metálica, bien el empleo de osteosíntesis reabsorbible, es la interferencia con las pruebas de imagen de la TC durante el seguimiento de procesos oncológicos. Esta cuestión dependerá del territorio craneofacial y del proceso patológico que nos ocupe y adquiere especial relevancia en la patología tumoral de la base craneal. En estos casos, y dado que los requerimientos biomecánicos del área lo permiten sin riesgos añadidos, la fijación con implantes reabsorbibles resultaría electiva. El perfil de los implantes a emplear en el tercio medio facial (miniplacas) minimiza estos efectos, por lo que cabe individualizar nuestra elección en función de las necesidades biomecánicas y funcionales de cada paciente y de la presencia de radioterapia adyuvante. A nivel mandibular, la necesidad de una osteosíntesis durante el procedimiento quirúrgico suele ir asociada a un estadio avanzado de la enfermedad oncológica y por lo tanto a la presencia casi inevitable de la radioterapia. En estas circunstancias se impone una fijación segura, suficientemente estable, habitualmente rígida, que proporcione una rehabilitación funcional lo más precoz posible y minimice la posibilidad de complicaciones; En la actualidad, los implantes reabsorbibles no garantizan estas premisas, por lo que resulta electiva la osteosíntesis con titanio aún asumiendo el inconveniente del posible retraso en el diagnóstico de una recidiva por interferencia con las pruebas de imagen de la TC. Ciertamente, desde la incorporación de la RM a nuestro arsenal diagnóstico rutinario esta desventaja ha quedado obviada, dado que los implantes de titanio no provocan interferencias ni artefactos en este tipo de exploraciones, tan solo una señal de vacío que se limita a la exacta localización y dimensión del implante; y es que las aleaciones de titanio no poseen magnetismo residual y los implantes por tanto pueden ser sometidos de forma rutinaria a Resonancias Magnéticas Nucleares (la permeabilidad magnética, en el caso de materiales poco permeables, puede ser medida con un instrumento denominado Severn Gauge cuya prueba de calibrado más baja es igual a 1.01, habiendo sido registradas permeabilidades menores en la aleación TAN).
El seguimiento de los procesos de consolidación y mineralización de fracturas u osteotomías no plantea ningún inconveniente, ya que las exploraciones TC con ventana ósea no se ven artefactadas por los implantes de titanio, ni por supuesto las exploraciones radiológicas simples o tomográficas.
Persiste la controversia en el caso de pacientes en crecimiento aunque en general, como después veremos, se tiende a retirarlas aunque no estén dando problemas invocando la incertidumbre sobre posibles efectos adversos a muy largo plazo.
Es bien conocido el fenómeno migratorio que acontece durante el crecimiento. Las osteosíntesis metálicas en el territorio craneal, por este motivo, deben de ser retiradas sistemáticamente, debido a su posible penetración endocraneal con la consiguiente interacción meníngea. La indicación de osteosíntesis reabsorbible en estos casos resulta electiva.
Fractura de la placa
Las placas pueden «fracturarse». La causa es la denominada fatiga metálica (Pohler y Straumann-1975), situación que acontece cuando la placa soporta una carga mecánica excesiva y prolongada, casi siempre por ausencia de reconstrucción ósea subyacente (placas de reconstrucción con puenteo del defecto óseo). Si la placa además ha sido excesivamente manipulada durante el proceso de moldeado, este fenómeno puede verse favorecido.
Pero la causa más frecuente de esta rotura metálica es el error en su elección, es decir, cuando le exigimos a una placa unas prestaciones biomecánicas para las que no está diseñada. En la actualidad, esta situación se presenta frecuentemente en el tratamiento de fracturas en mandíbulas edéntulas con miniplacas, en las que subestimamos las fuerzas funcionales que han de contrarestar.
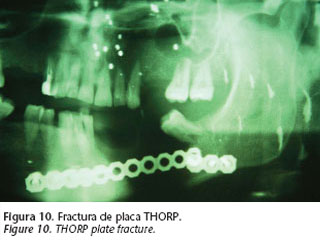
De otra parte, cuando los defectos en la continuidad ósea no son restaurados, los extremos óseos remanentes tienden a reabsorberse, por lo que a largo plazo pueden producirse aflojamientos y suelta de tornillos, inicialmente estables y osteointegrados, que deberán ser retirados.
Osteosíntesis con titanio en niños
Afortunadamente, la gran mayoría de las fracturas de los maxilares que acontecen en la edad pediátrica son subsidiarias de tratamiento conservador, entendiéndose como tal desde la abstinencia terapéutica a la fijación intermaxilar. La elección de una u otra alternativa depende de las características intrínsecas de la fractura y de la edad del paciente, sobre todo en lo que se refiere a la etapa de dentición que presenta. En otras ocasiones es precisa una cirugía abierta para la reducción de la fractura, aunque finalmente no sea imprescindible la fijación interfragmentaria. En estos casos el exquisito manejo quirúrgico de los tejidos blandos es imperativo para minimizar el daño vascular y la posible repercusión que sobre el crecimiento é pudiera tener.
En general, se tenderá a ser más conservador a menor edad del enfermo, pero se presentan casos en la práctica clínica que no lo permiten. Hay situaciones en las que una reducción abierta con fijación activa de los focos resulta necesaria para una adecuada curación de las fracturas, fundamentalmente en los casos con un importante grado de desplazamiento, en presencia de focos múltiples y/o de fracturas de ambos maxilares y con independencia del grupo etario del paciente (Fig. 11). Clásicamente se ha utilizado la osteosíntesis alámbrica (acero inoxidable) para solventar la mayoría de estas situaciones, asociada o no a fijación intermaxilar. La evolución en el diseño de miniplacas y microplacas de titanio, con perfiles muy bajos (1-1,5 mm) y tornillos muy cortos y autoroscantes, ha generalizado su uso en estas situaciones desplazando casi totalmente a la fijación alámbrica, ya que la estabilidad primaria que posibilita es muy superior, por lo que en muchas ocasiones se puede obviar la fijación intermaxilar, situación nada despreciable tratándose de niños.
En el caso de las fracturas mandibulares el objetivo final del tratamiento es similar al de la población adulta, esto es, obtención de una reducción anatómica y de una estabilización del foco que permita una correcta e inmediata reparación, tanto anatómica como funcional. Partiendo de esta premisa, es evidente que la mandíbula de estos pacientes esta sometida a una serie de particularidades, en gran parte comunes al resto del esqueleto facial, que condicionan la solución terapéutica: hueso en crecimiento, crecimiento combinado máxilo-mandibular, presencia de gérmenes dentarios (distintas fases de dentición) y posición basal del nervio dentario inferior. La dinámica del crecimiento conduce por lo tanto a encontrarnos con diferentes situaciones clínicas en el tratamiento quirúrgico de las fracturas mandibulares en niños. Esta heterogeneidad, unida a la baja incidencia de fracturas faciales en la infancia, justifica la inexistencia de un tratamiento consensuado. Como principios básicos, el grado de desplazamiento va a condicionar la necesidad de osteosíntesis, la fase de la dentición determinará las técnicas de inmovilización y de osteosíntesis a emplear y la localización de la fractura la duración de la inmovilización (Hardt-Gottsauner-1993).
Las ventajas de la cirugía abierta con fijación no sólo se fundamentan en la obtención de una reducción precisa de los focos de fractura. Con este tipo de actuación se posibilita que la vía aérea permanezca permeable, saliendo al paso de potenciales complicaciones graves como la aspiración de vómito (nada infrecuente en niños), y consiguiéndose un rápido retorno a la dieta habitual del niño, con mantenimiento del funcionalismo máxilo-mandibular y cráneo-mandibular (ATM) de forma precoz; esta fisioterapia pasiva es beneficiosa para todo el sistema estomatognático en crecimiento.
Los inconvenientes descritos en la literatura incluyen el posible daño de los gérmenes dentarios, la interrupción del potencial osteogénico del periostio al exponer la mandíbula con la consiguiente alteración del patrón de crecimiento, aparición de cicatrices hipertróficas, fundamentalmente en adolescentes, y la posible interferencia del material de osteosíntesis en el crecimiento mandibular a la que nos referiremos más tarde. Hay que destacar que todos estos inconvenientes, salvo el último, son comunes para los sistemas de osteosíntesis reabsorbible, e incluso podría pensarse que algo más acentuados debido a los mayores perfiles de sus placas y tornillos. (Champy-1992).
Las indicaciones para la cirugía abierta con fijación semirígida en las fracturas mandibulares de la infancia son, en nuestra opinión y en concordancia con otros autores las siguientes:
1. Traumatismos de elevada energía, que originan fracturas mandibulares múltiples, especialmente si se acompañan de fracturas del tercio medio facial. Dentro de este apartado se incluyen las fracturas abiertas. La energía liberada origina frecuentemente la conminución de los fragmentos; la fijación con miniplacas permite recuperar la arquitectura de la mandíbula minimizando el daño funcional y estético.
2. Deficiente fijación de las férulas metálicas del bloqueo intermaxilar. Durante los dos primeros años de vida los dientes deciduos no aportan la suficiente estabilidad. Posteriormente, la dentición mixta dificulta en ocasiones la obtención de una adecuada inmovilización. La reducción abierta en fracturas mandibulares, únicas pero con importante desplazamiento, permite evitar una fijación intermaxilar precaria.
3. Asociación de fracturas de cóndilo y del cuerpo mandibular. Fundamentalmente antes de los 12 años, el cóndilo constituye la localización más frecuente de las fracturas mandibulares. El tratamiento conservador, basado en dieta blanda y movilización precoz, se ve entorpecido en ocasiones por la existencia de otro foco de fractura, fundamentalmente en el cuerpo mandibular contralateral. La fijación con material de osteosíntesis permite la apertura oral precoz, minimizando el riesgo de anquilosis en la articulación dañada .
4. Situaciones en que las consecuencias del traumatismo no se limiten a las fracturas faciales. En las primeras etapas de la infancia resulta desgraciadamente habitual la presencia de lesiones intracraneales o tóraco-abdominales. En estas situaciones, resulta aconsejable recurrir al tratamiento abierto de las fracturas mandibulares, que permite reducir y estabilizar adecuadamente la fractura, manteniendo libre la vía aérea, lo que facilita el trabajo en las unidades de cuidados intensivos pediátricas y evita la indeseable traqueotomía .
En el caso de fracturas orbitomalares desplazadas, mucho más infrecuentes, se aconseja un abordaje intraoral y fijación mediante miniplaca de titanio en el arbotante máxilo-malar. Si se precisa un abordaje del reborde infraorbitario o del suelo de la órbita se puede utilizar una vía subtarsal o transconjuntival. El reborde infraorbitario puede estabilizarse mediante osteosíntesis alámbrica o mediante microplacas de titanio. El suelo de la órbita puede restaurarse mediante reducción pura del fragmento desplazado, o mediante injertos autólogos sin ningún tipo de fijación. Por último, si se precisa un abordaje en cola de ceja para realizar una osteosíntesis fronto-malar, se pueden emplear mini-microplacas de titanio o bien osteosíntesis alámbrica si es que el arbotante máxilo-malar ha sido convenientemente fijado. En las fracturas tipo Lefort, a pesar de su infrecuencia, la mayor parte de los casos (80%) precisan de cirugía abierta y fijación semirígida. Sólo aquellos casos con mínimo desplazamiento son subsidiarios de una abstención terapéutica (dieta blanda y control) o de la aplicación de un bloqueo intermaxilar durante 3 semanas. En el resto de los casos se procederá a la estabilización de los arbotantes naso-maxilares y máxilo-malares mediante miniplacas.
En la actualidad, tanto para las fracturas orbitomalares como para las de tercio medio, la indicación de osteosíntesis reabsorbible puede resultar electiva, ya que sus resultados son equiparables a la osteosíntesis con titanio y se obvia la posibilidad de una futura retirada. La decisión creemos depende, sobre todo, de la experiencia del cirujano con uno y otro sistemas. Con respecto a las fracturas órbito-naso-etmoidales, hay que considerar que el crecimiento del tercio medio facial está condicionado por el desarrollo de la fosa craneal anterior, órbita y septo. Las fracturas de esta región, aunque infrecuentes, tienen por un lado un alto potencial de alterar el desarrollo facial, pero por otro pueden acompañarse de importantes secuelas estéticas ante una reducción inapropiada. Por ello, a pesar de la importante desperiostización que conlleva su tratamiento, la mayor parte de los autores mantienen la idea de realizar una reducción anatómica de todas las fracturas desplazadas mediante abordaje coronal en ausencia de heridas faciales que permitan un abordaje directo. La fijación semirrígida se hará preferentemente con miniplacas reabsorbibles (si es que las condiciones de los tejidos blandos lo permiten) con alambres de acero, con microplacas de titanio o si la estabilidad de la fractura lo permite, con pegamentos biológicos (cianoacrilato). La utilización de placas metálicas en este territorio conlleva cierto riesgo de migración intracraneal, y requiere de un seguimiento estrecho hasta finalizado el crecimiento y si es necesario de un segundo abordaje para su retirada.
Conclusiones
Se ha invocado de forma reiterada en la literatura la interferencia de la osteosíntesis de titanio en el crecimiento de los huesos faciales.Como ya apuntábamos, es difícil discriminar entre los efectos deletéreos que sobre el crecimiento se derivan de la propia fractura, del traumatismo indirecto sobre la ATM, de las lesiones sobre tejidos blandos, traumáticas o quirúrgicas (matriz de crecimiento de Moss y Rankow) y los consecuentes a la aplicación de miniplacas de titanio para la osteosíntesis.
La fijación con miniplacas y microplacas de titanio, excluido el territorio pericraneal, plantea pues la controversia derivada de la necesidad de una segunda intervención para su retirada, necesidad que se argumenta para indicar la fijación con sistemas reabsorbibles. Los autores que mantienen tal postura suelen proceder a su retirada a los 2-3 meses de su aplicación. Cuando los abordajes son intraorales las consecuencias de una segunda cirugía pueden considerarse como asumibles, pero en abordajes extraorales (p.e. coronal o submandibular) estas consecuencias no pueden ser desdeñadas. De otra parte, algunos cirujanos postulan que el nuevo abordaje quirúrgico repercute sobre el crecimiento facial de manera similar al tratamiento primario de la fractura, por lo que teniendo en cuenta la reconocida biocompatibilidad de las placas de titanio recomiendan su mantenimiento, sobre todo en pacientes mayores de 13 años, salvo que produzcan alguna alteración objetiva. Hay que tener en cuenta, como ya hemos dicho, que las osteosíntesis se manifiestan biomecánicamente activas hasta que la fractura ha consolidado; a partir de este momento se comportan como cuerpos inertes sobre los cuales, y en ausencia de complicaciones, se produce remodelado óseo y osteointegración, pudiendo evidenciarse como el material «acompaña» a la mandíbula en su crecimiento.
Siguiendo los postulados de Medicina Basada en la Evidencia, no existe en la literatura evidencia científica contrastada que establezca una relación causal directa entre la presencia de un implante de titanio y una alteración del crecimiento sobre un hueso facial. La experiencia clínica de muchos cirujanos, entre los que nos encontramos, habla en contra de esta posibilidad, por lo que una vez realizada la pertinente valoración crítica en términos de validez y utilidad, podemos concluir que esta hipótesis no justifica la no utilización de estos implantes en niños cuando sea necesario, ni la sistemática retirada de los mismos cuando no lo sea.
En cualquier caso, un seguimiento prolongado es imprescindible en estos pacientes sobre los que se individualizará la decisión.
Materiales reabsorbibles
La utilización de placas reabsorbibles en cirugía craneofacial pediátrica es rutinaria en la actualidad, habiendo desplazado al titanio por sus efectos adversos. El material metálico no es ideal porque pueden provocar alteración del crecimiento de la bóveda craneal y algunos autores recomiendan retirarlos.23 Por otra parte es muy difícil su utilización en cráneos menores de 6 meses por su debilidad.
Se han documentado placas y tornillos palpables en zonas de piel fina; ocasionalmente extrusión a través de la piel; casos infrecuentes de infección secundaria a reacción a cuerpo extraño. Sin embargo, la mayor importancia se centra en la migración de las placas a través de la duramadre, en un porcentaje importante; más frecuente en la región temporal y en los casos sindrómicos.
Por otro lado, la fijación rígida permanente en un cráneo en crecimiento puede ocasionar por sí misma la aparición de deformidades residuales. Numerosas publicaciones avalan el uso y buen resultado de las miniplacas reabsorbibles en este tipo de pacientes.
La utilización de placas reabsorbibles en trauma craneofacial está menos documentada que en cirugía craneofacial de deformidades pero es suficiente para comprobar su utilidad. Eppley y Prevel publicaron en 1997 su experiencia en fracturas del tercio medio facial con el uso de Lactosorb en 30 pacientes. Con un seguimiento mayor de un año, observó una cicatrización adecuada y sin reacciones adversas, aunque el autor recomienda no usarla en fracturas de fragmentos pequeños y finos. Resultados similares fueron publicados por Enislidis y cols en una serie de 27 fracturas maxilomalares.

Ylikontiola y cols han utilizado placas reabsorbibles para la osteosíntesis de fracturas parasinfisarias mandibulares de 10 adultos, con buenos resultados (un paciente sufrió exposición intraoral de una placa, que precisó su extirpación parcial). Estos autores recomiendan buena cobertura de tejidos blandos para evitar la exposición de las placas. Otros autores34 también han publicado buenos resultados en fracturas mandibulares.
Tams y cols,35 en un estudio experimental, han comprobado que las fracturas de ángulo mandibular pueden tratarse de forma eficaz con 2 placas reabsorbibles colocadas sobre la línea oblicua externa y el tercio medio vestibular de la mandíbula, respectivamente.
Hoffmann y cols36 utilizaron placas PDLLA (Resorb X) en 22 pacientes tratados de trauma craneofacial, osteotomía Le Fort I y síndromes craneofaciales, no habiendo observado complicaciones en la cicatrización (clínica y radiológica).

Suuronen y cols,1 en un estudio retrospectivo de más de 200 pacientes tratados con fijación reabsorbible en varias aplicaciones de cirugía craneomaxilofacial a lo largo de 7 años, sostienen que las placas reabsorbibles pueden utilizarse de rutina en la osteosíntesis maxilofacial.
La otra gran aplicación de las placas reabsorbibles es la cirugía ortognática. En este campo la literatura se incrementa constantemente con numerosos artículos documentando su uso. Haers y cols,37 publicaron en 1998 el primer caso de cirugía bimaxilar y mentoplastia simultáneas fijadas exclusivamente con material reabsorbible. Turvey y cols, han publicado su experiencia en 70 pacientes de cirugía ortognática bimaxilar con seguimiento a corto plazo (6-24 meses). Tres pacientes tuvieron problemas con la pérdida de tornillos pero la estabilidad y la oclusión fueron adecuadas en todos los pacientes.
Norholt y cols, han comparado el uso de placas reabsorbibles Lactosorb®y de titanio en la osteosíntesis de Le Fort I, en un estudio randomizado y prospectivo sobre 60 pacientes, en relación con la estabilidad y morbilidad. Estos autores, han observado un cambio vertical medio de 0,6 mm a las 6 semanas postop® en el grupo reabsorbible (cambio estadísticamente significativo, medido con implantes metálicos colocados en el hueso), no encontrando cambios significativos en el grupo de titanio. Este cambio no fue clínicamente aparente y no se observó en los siguientes controles radiológicos, habiendo completado satisfactoriamente la consolidación ósea todos los pacientes. Hubo 2 casos de infección y dehiscencia de herida con las placas reabsorbibles, mientras que en el grupo de titanio se palpaban más frecuentemente las placas 6-12 meses después y 3 casos requirieron su retirada.
Matthews y cols, han estudiado la estabilidad de los tornillos SR-PLLA reabsorbibles en la osteosíntesis de la osteotomía sagital mandibular de avance en 11 pacientes, comparándola con una cohorte de 11 pacientes sometidos a la misma osteotomía fijada con titanio, y no han encontrado diferencias significativas entre ambos grupos al comparar la estabilidad cefalométrica con seguimiento de un año. Otros estudios sobre osteotomías Le Fort I y osteotomía sagital mandibular han mostrado la ausencia de complicaciones. 40-43
Ferretti y Reyneke, han publicado un estudio prospectivo comparativo sobre 40 pacientes con clase II sometidos a osteotomía sagital mandibular, en el que han comparado la estabilidad a largo plazo y las complicaciones entre la fijación con tornillos de titanio y tornillos de P(L/DL)LA 82:18, y no han encontrado diferencias significativas entre ambos grupos.
El grupo de Helsinki ha mostrado su experiencia en cirugía ortognática durante 8 años, con seguimientos de más de 5 años, con resultados excelentes. Recientemente han publicado su experiencia en cirugía ortognática en un periodo de 10 años (1991-2001) en un estudio retrospectivo sobre 163 pacientes y 329 osteotomías. La aceptación de los pacientes ha sido excelente y la incidencia de complicaciones observadas fue muy baja, sin afectar el resultado final en ningún caso: 8,6% de complicaciones menores, 0,6% (un caso) de infección y 1,8% (3 casos) de mordida abierta postoperatoria, que ocurrió con los dispositivos antiguos en la primera fase del estudio.
Fuente del Campo, ha publicado recientemente en un estudio multicéntrico, su experiencia en osteosíntesis maxilofacial con material reabsorbible (SR-PLLA) en 208 casos, de los cuales 142 correspondían a cirugía ortognática, con un seguimiento máximo de 8 años. Este autor ha observado una tasa de complicaciones del 7,9%: 2 casos de inestabilidad maxilar por mala técnica, 6 casos de granuloma, 4 casos de exposición de placa y otros 4 de desplazamiento de la misma, siendo la mayor parte de estas complicaciones atribuidas a la técnica y no al material empleado.
Parece claro que en cirugía ortognática el material reabsorbible es una alternativa absolutamente válida al titanio.
Ventajas y desventajas de la osteosíntesis reabsorbible
La literatura revisada muestra en general que las placas reabsorbibles son una alternativa válida al titanio en la mayor parte de las osteosíntesis craneomaxilofaciales. Se publican mayores índices de complicaciones en las series pequeñas, que suelen corresponder a la primera fase de utilización de estos materiales. Algunos problemas permanecen sin resolver, como la biodegradación prolongada. 47 Otro problema es la palpabilidad de la placas. Gerlach,48 utilizando placas reabsorbibles en el tratamiento de fracturas malares, observó que se palpaban después de 2 años a través de la piel. También observó que de 15 pacientes tratados, 2 presentaron una reacción inflamatoria no infecciosa a los 30 meses. Por otra parte Bergsma y cols,15 observaron en su serie que todos los pacientes desarrollaron una reacción a cuerpo extraño en la zona operatoria 3 años después. Se encontraron fragmentos de LPLA durante la exploración quirúrgica hasta 5,7 años más tarde.

Hay que señalar que estas publicaciones corresponden a las fases iniciales de utilización de la osteosíntesis reabsorbible.
El material reabsorbible ideal debe soportar los fragmentos óseos durante el periodo de curación y además reabsorberse en su totalidad cuando éste se ha completado, sin que los metabolitos resultantes causen ninguna alteración local o sistémica.12 Estas características proporcionan indudables ventajas sobre todo porque no precisan su extracción. Se ha publicado un 11,1% de pacientes que precisaron la extracción de las placas de titanio en cirugía ortognática, 49 y del 11,5% en fracturas mandibulares.50 Por otra parte es particularmente ventajoso en países donde habitualmente se retira postoperatoriamente el material de osteosíntesis, lo que conlleva anestesia general, morbilidad y coste económico. También se evitan las interferencias que el titanio puede producir con procedimientos radiológicos,2 y la sensibilidad térmica.51
Análisis de las desventajas de la osteosíntesis con material reabsorbible:
• Propiedades físicas. Uno de los inconvenientes es el grosor de las placas. Para la misma resistencia se necesita mayor grosor de las placas reabsorbibles. Esto es un inconveniente en algunas localizaciones y situaciones específicas. Otro problema es la difícil aplicación en fracturas conminutas y huesos muy finos. En estas condiciones es difícil adaptar estas placas por lo que puede ser una contraindicación. Si se doblan demasiadas veces, algunos autores,52 señalan que el procedimiento de calentado puede hacer perder sus propiedades mecánicas aunque esto también supone un problema con el titanio.
• Curva de aprendizaje. El manejo y adaptación de estas placas es más engorroso que al que estamos habituados con el titanio, por lo que inicialmente el tiempo quirúrgico es mayor. Esto es debido al proceso de calentado y la necesidad de terrajado del orificio que requiere la mayoría de los sistemas; el desarrollo de pistolas para introducir los tornillos en el agujero sin necesidad de terrajado ha posibilitado disminuir el tiempo quirúrgico sin perjuicio de sus propiedades mecánicas. Esto ha sido demostrado tanto en estudios experimentales,53 como clínicos,54. Sin embargo, es difícil su uso en huesos muy finos por la posibilidad de fractura.55
Esto requiere una curva de entrenamiento inicial para familiarizarse con el material,45 aunque hoy por hoy la calidad de manejo es inferior al titanio; sin embargo, esto no compromete el resultado final.
• Manejo en cirugía ortognática. El atornillado de la osteotomía sagital mandibular es idéntico con titanio o reabsorbible, únicamente se requieren unos segundos más para el terrajado de los orificios. En el maxilar, la movilidad inicial, durante 4-5 semanas, puede parecer preocupante, sobre todo en los segmentados, pero realmente no lo es y no hay problema de estabilidad al cabo de ese periodo.45 Otro aspecto que entraña cierta dificultad es la colocación de las miniplacas en la premaxila en la osteotomía de los Le Fort segmentados. Actualmente se está trabajando en el desarrollo de placas preformadas reabsorbibles para los avances maxilares (tipo Lindorf o Prebent); esto hará la colocación de la osteosíntesis maxilar tan sencilla como el titanio. Un aspecto ya mencionado es la palpación de las placas en el reborde infraorbitario, que no es un problema actualmente.
• No visualización de los tornillos en las placas radiográficas. Esto ocasionalmente puede dificultar actitudes diagnósticas cuando hay problemas de consolidación, etc.45
• Se necesita una cobertura adecuada de partes blandas para que no haya exposición de las placas ya que el proceso de degradación de las mismas se altera. En estos casos es necesario retirarla después del periodo de consolidación ósea.
• Versatilidad de las miniplacas. Algunas compañías solo disponen de un único sistema, no válido para todas las osteosíntesis. Generalmente estos sistemas no están indicados en osteosíntesis mandibular o situaciones que requieren mayor resistencia. Así, Dolanmaz y cols,56 aconsejan la fijación intermaxilar en el postoperatorio inmediato tras comparar experimentalmente en ovejas la estabilidad de las placas reabsorbibles PLLA-PGA 82:18 y de titanio en la osteosíntesis de la osteotomía sagital mandibular con un avance de 5 mm.
• Coste. Actualmente el coste de la osteosíntesis reabsorbible es 2- 3 veces superior a la osteosíntesis con titanio. Sin embargo, si tenemos en cuenta el coste de la extracción del titanio, en un porcentaje no despreciable, y de que en algunos países es rutinaria su retirada, es evidente que es más barato que el titanio. Por otra parte en algunos países, y próximamente en el resto de la CEE, el estocaje del material de osteosíntesis de titanio será igual al reabsorbible, es decir, envasado en paquetes de una o varias unidades, no en un embalaje común como hasta ahora), lo que hará encarecer el producto. También es de esperar que con la mayor popularización del material reabsorbible el precio tienda a la baja.
Conclusiones
La utilización de placas y tornillos reabsorbibles en la osteosíntesis craneomaxilofacial es cada día más frecuente. La literatura demuestra que es una alternativa válida a la osteosíntesis con titanio en la mayoría de las situaciones clínicas. Actualmente, presentan todavía algunas desventajas en relación con el titanio, como la mayor incomodidad de uso y el coste económico. Si excluimos las fracturas con fragmentos finos y conminutos y algunas situaciones específicas, el material reabsorbible puede sustituir al titanio en la osteosíntesis craneomaxilofacial actual. Únicamente es necesaria experiencia para superar la curva de aprendizaje inicial que hace su utilización más incómoda.
Por otra parte, son necesarios estudios para comparar entre sí los distintos sistemas reabsorbibles ya que la composición, y por lo tanto sus características, varía de unos a otros.
FRACTURAS DE LA DIAFISIS FEMORAL
PRIMERA SECCION. PATOLOGIA TRAUMATICA
Capítulo Primero. Fracturas. Fracturas del Miembro Inferior.
FRACTURAS DE LA DIAFISIS FEMORAL
Capítulo Primero. Fracturas. Fracturas del Miembro Inferior.
FRACTURAS DE LA DIAFISIS FEMORAL
Hechos anatomicos importantes
- La diáfisis femoral se extiende desde un plano horizontal a 3 cm por debajo del trocánter menor, hasta la zona esponjosa supra condílea.
- Se encuentra envuelta por potentes masas musculares que toman inserción amplia a lo largo de todo el cuerpo del hueso.
Ello le confiere una excelente vascularización que favorece la rápida formación del callo óseo. Pero la acción potente de los músculos que en ella se insertan, son los responsables, en gran parte, de los grandes desplazamientos que con frecuencia se encuentran, así como de la difícil reducción e inestabilidad de los fragmentos óseos. - Muy cercanos al cuerpo del hueso se encuentran los vasos femorales; los segmentos óseos desplazados con facilidad pueden comprimir, desgarrar o seccionar la arteria o vena femorales. Particularmente peligrosas son, a este respecto, las fracturas del 1/3 inferior de la diáfisis (o supracondíleas).
- La rica irrigación de la diáfisis femoral, así como la de las grandes masas musculares al ser desgarradas por los segmentos fracturados, pueden generar una hemorragia cuantiosa (1 ó 2 litros), generando una brusca hipovolemia, transformando así al fracturado en un accidentado grave, con los caracteres propios de un politraumatizado.
Generalidades
Contrariamente a lo que ocurre con la fractura del cuello del fémur, la lesión es frecuente en enfermos jóvenes, adultos y niños.
Necesariamente se requiere de una fuerza muy violenta para fracturar la diáfisis femoral; por ello es dable sospechar graves lesiones de partes blandas (músculos), apreciables desplazamientos de fragmentos óseos, con riesgos de lesiones vasculares o de troncos nerviosos, o bien lesiones viscerales o esqueléticas de otros segmentos (pelvis, columna vertebral).
Clasificacion
Fracturas simples: aquéllas en las cuales la lesión se reduce a la fractura diafisiaria, sin otra complicación vascular, nerviosa, hemodinámica o visceral.
Fracturas complejas: por el contrario, la fractura se acompaña de lesiones de otro tipo: fractura de pelvis; de columna; viscerales: ruptura hepática o esplénica; lesiones toraco-pulmonares; intensa hemorragia focal con trastornos hemodinámicos; traumatismos encéfalo-craneanos, etc.
En este tipo de fracturas, la complicación anexa debe ser diagnosticada con rapidez y la resolución de la complicación puede tener mucho más urgencia que la de la fractura misma.
Todos estos enfermos deben ser considerados como politraumatizados graves y su terapéutica debe ser ajustada a esta condición.
Diagnostico
En general no constituye problema. El antecedente del traumatismo violento, dolor intenso y la frecuente e importante deformación del muslo, son hechos indisimulables. Con frecuencia están presentes todos los signos propios de las fracturas diafisiarias.
Procedimiento diagnóstico
a. Anamnesis: referida a antecedentes sobre naturaleza del accidente, magnitud, etc.; de ello puede deducirse la posibilidad de la existencia de otras lesiones anexas, quizás más graves que la fractura misma.
b. Examen físico completo:
Inspección: buscando deformación del muslo, pérdida de los ejes, aumento de volumen a tensión (hematoma de fractura o lesión vascular importante); existencia de heridas (fractura expuesta), etc.
- Valores vitales.
- Examen segmentario: cabeza, cuello, tórax, abdomen, pelvis y extremidades, con el fin de detectar lesiones anexas.
- Examen del miembro lesionado.
Examen vascular periférico: temperatura de tegumentos, color, pulsos periféricos, dolor, etc.
Examen neurológico: buscar indemnidad sensitiva en terreno del ciático.
Radiología: la confirmación diagnóstica debe ser hecha de inmediato, tan pronto se ha resuelta la inmovilización provisoria, conseguida ya sea por una férula de Braun y tracción continua, férula de Thomas o yeso pelvipédico, según sean las circunstancias y posibilidades.
La radiografía debe comprender el fémur en toda su extensión; no son infrecuentes fracturas de doble foco, con luxación de cadera. La radiografía limitada sólo al sector diafisiario de la fractura, puede hacer pasar inadvertida la verdadera complejidad de la lesión. Ante la menor sospecha de lesión pelviana, el estudio debe extenderse a una radiografía de pelvis y columna vertebral.
Desplazamiento de los fragmentos: los desplazamientos de los fragmentos óseos son frecuentes, determinados por la fuerza del impacto o por la acción de las potentes masas musculares que en ellos se insertan. La acción contracturante de los músculos determina a su vez las dificultades para la reducción y contensión de la fractura.
Según sea el nivel de la fractura y en relación a las zonas de inserción de los músculos, las desviaciones de los fragmentos suelen ser muy características: en fractura de la parte alta de la diáfisis, el fragmento proximal se encuentra en flexión anterior por acción del músculo psoas-ilíaco, en abducción y rotando al externo por acción de los músculos pelvi-trocantéreos.
En las fracturas del tercio inferior, el fragmento distal se encuentra desplazado hacia atrás por acción de los músculos gastro-necmios; en esta angulación posterior del segmento óseo no son infrecuentes las lesiones por compresión, desgarro o sección de la arterial femoral o poplítea.
En las fracturas del tercio medio de la diáfisis, el segmento proximal es desplazado hacia medial por acción de los aductores.
Tratamiento
Es importante considerar el tratamiento de estas fracturas en tres momentos diferentes: en cada uno de ellos, los objetivos son distintos.
1° fase: De suma urgencia: se realiza en el sitio mismo del accidente y el objetivo es:
2° fase: De urgencia: Aquí los objetivos son más complejos y las exigencias médicas son mayores.
- Alinear el eje del muslo corrigiendo la angulación y rotación; si fuese posible, también corregir el acabalgamiento.
Se consigue con una tracción suave, sostenida pero con firmeza; todas las maniobras deben ser realizadas con suavidad, calma y en forma lentamente progresiva.
Si así se procede, el procedimiento es poco doloroso.- Inmovilizar el miembro inferior, fijándolo a un vástago rígido (esquí, tabla, etc.) que debe llegar desde la pared del tórax hasta el tobillo. Si no se cuenta con ningún elemento de sostén, se fija al miembro sano, vendando el uno al otro en toda su extensión.
Especialmente útil resulta el empleo de la férula de Thomas; con ella se consigue inmovilizar los fragmentos, controlar la rotación y agregar la tracción con lo que se corrige el acabalgamiento.- Analgésicos: idealmente inyectables (morfina).
- Importante es consignar y hacer llegar al médico tratante:
- Fecha y hora del accidente.
- Valores vitales detectados en el momento de la atención.
- Existencia y magnitud de las desviaciones de los ejes (angulación, acortamiento, rotación, etc.).
- Alteración de los pulsos periféricos.
- Estado de la sensibilidad.
- Color y temperatura de los tegumentos del miembro afectado.
- Medicación administrada.
- Orden de traslado urgente a un centro asistencial.
3° fase: Tratamiento definitivo: los objetivos que se persiguen con el tratamiento definitivo no son fáciles de cumplir, y deben quedar reservados para el especialista. El médico general, con escasa experiencia, no debe intentar resolver el problema con ninguno de los métodos posibles de usar. Aún más, el especialista que no cuente con una infraestructura de pabellón aséptico, servicio de radiografía intraoperatoria, anestesistas competentes, transfusión inmediata, set de instrumental completo, tampoco debe intentar la resolución del problema, sobre todo si pretende hacerlo con un acto operatorio.
- Examen clínico completo, procurando detectar alteraciones generales o sistémicas propias de un estado de shock.
- Preparar vías endovenosas para infusión de soluciones hidrosalinas (suero gluco-salino, Ringer-lactato).
- Transfusión sanguínea según sea el caso.
- Analgesia endovenosa.
- Examen muy cuidadoso del estado vascular y neurológico del miembro fracturado.
- Tracción continua, idealmente transesquelética, desde la tuberosidad anterior de la tibia.
- Examen radiológico de fémur; se extiende a pelvis, columna, tórax, cráneo, según sean las circunstancias (polifracturado).
- Hospitalización y colocación de férula de Braun con 7 a 8 kg de peso aproximadamente.
- Disponer el traslado cuando los valores vitales estén estabilizados, si el centro asistencial no cuenta con la infraestructura adecuada para el tratamiento definitivo.
El traslado, en estas circunstancias, no es urgente.
Las complicaciones intra y post-operatorias suelen ser muy frecuentes y sus consecuencias son desastrosas.
La más elemental prudencia aconseja, en estas circunstancias, derivar al enfermo a un servicio mejor dotado.
La reducción, inmovilización y contensión de los fragmentos hasta su consolidación definitiva, pueden ser obtenidos con dos tipos de procedimientos.
Tratamiento ortopédico
Pueden ser realizados con tres técnicas diferentes:
1. Reducción inmediata en mesa traumatológica, bajo control radiológico e inmovilización con yeso pelvipédico.
Corresponde a un procedimiento poco usado; la reducción suele ser muy difícil y generalmente es inestable, sobre todo en fracturas desplazadas del 1/3 superior o inferior del fémur, sometidas a violentas tracciones musculares.
Generalmente es un procedimiento usado como una forma provisoria de inmovilización, cuando procede realizar el traslado del enfermo. Sin embargo, no debe ser desechada del todo, sobre todo si se trata de enfermos jóvenes y se ha logrado una reducción y una estabilización correcta y mantenida.
2. Tracción continua: seguida de un yeso pelvipédico, una vez que se ha conseguido la formación de un callo que, aunque no definitivo, asegure la contensión de los fragmentos en vías de consolidación.
El procedimiento libera al enfermo de la tracción y le permite continuar el tratamiento en su domicilio.
Como el procedimiento obliga a un control radiográfico periódico mientras permanece con la tracción, sólo puede ser realizado en servicios que posean aparatos de rayos portátiles.
Si no se cuenta con este servicio, el tratamiento no se puede realizar.
3. Tracción continua mantenida hasta que el callo óseo esté sólidamente formado. Especialmente usado en enfermos jóvenes, en que el plazo de consolidación es breve; el foco de fractura debe estar bien reducido y estable.
También obliga necesariamente a un periódico control radiográfico.
Los tres métodos ortopédicos señalados, especialmente los dos últimos, fueron intensamente usados hasta el advenimiento de los procedimientos quirúrgicos, especialmente el enclavado intramedular de Küntscher. Sin embargo, en todos los servicios del mundo se está reconsiderando la situación y el procedimiento ortopédico que ya parecía olvidado definitivamente, está volviendo a reactualizarse como un procedimiento al cual se puede recurrir en determinadas circunstancias.
El empleo del procedimiento ortopédico debe ser cuidadosamente considerado en cada caso particular. Implica hospitalización prolongada, someterse a procedimientos a veces mal tolerados y debido a la inmovilización prolongada, rigideces articulares especialmente de rodilla a veces definitivas.
Indicaciones de tratamiento ortopédico
- Fracturas diafisiarias en fémur en el niño.
- Fracturas conminutas.
- Infección de partes blandas.
- Negativa tenaz del enfermo o de sus familiares a ser operado.
Indicaciones relativas
- Fracturas bien reducidas y estables.
- Enfermos jóvenes.
- Enfermos con patología anexa (cirrosis hepática descompensada, etc.).
- Infraestructura quirúrgica inadecuada, no existiendo posibilidad razonable de traslado.
- Cirujano no especializado, sin experiencia quirúrgica adecuada y sin posibilidad de traslado.
Tratamiento quirúrgico
Es el tratamiento de elección en el adulto en los servicios de la especialidad, al lograr una reducción anatómica y estable, permitiendo una rehabilitación precoz y hospitalización más breve.
Hechos propios de la fractura, del enfermo y sus circunstancias, progresos tecnológicos, han ido inclinando al médico a preferir acentuadamente los procedimientos quirúrgicos para el tratamiento de estas fracturas.
Fracturas de tratamiento quirúrgico:
Sin embargo, aun cuando la indicación de tratamiento quirúrgico sea inobjetable dadas las condiciones clínicas, el médico tratante debe considerar otras circunstancias no relacionadas directamente con el enfermo:
- Fractura con grandes desplazamientos de fragmentos.
- De muy difícil reducción.
- De contensión imposible, difícil o inestable.
- Necesidad de una rápida rehabilitación muscular y articular.
- Fracturas con compromiso vascular o neurológico.
- Fracturas expuestas.
- Fracturas en hueso patológico (metástasis, mieloma, etc.).
- Fracturas en enfermos de edad muy avanzada en que la postración implica un grave riesgo vital.
El resto de las fracturas de diferentes variedades, susceptibles de ser tratados por métodos ortopédicos, pueden ser operadas si no existen contraindicaciones de parte del enfermo, del ámbito quirúrgico, del cirujano, etc.
- Excelente infraestructura hospitalaria.
- Pabellones quirúrgicos estrictamente adecuados para una gran cirugía traumatológica.
- Muy buen apoyo radiográfico intra-operatorio.
- Equipo de ayudantes, anestesistas, servicio de transfusiones. Apoyo irrestricto a Servicio de Cuidados Intensivos.
- Set de instrumental completo para la ejecución de las técnicas a emplear.
Con frecuencia actúa en forma poderosa el deseo del enfermo y del cirujano de acceder con prontitud a una rápida rehabilitación física.
La tendencia quirúrgica en la solución de este tipo de fracturas se ha acentuado definitivamente, sobre todo después de la introducción del Clavo de Küntscher y de las placas de osteosíntesis.
Métodos operatorios: la modalidad técnica varía según sea la ubicación de la fractura:
Insistimos, cualquiera sean los métodos de osteosíntesis empleados, deben ser realizados bajo condiciones estrictas e intransables:
- Fracturas del 5° proximal de la diáfisis (sub-trocantéreas) requieren del uso de un clavo placa angulada que busca sujeción en cuello femoral y diáfisis.
- Fracturas del 5° distal (supra-condíleas) igualmente requieren de clavo-placa angulada que busca sujeción en la región condílea y en la diáfisis (placas condíleas).
- Fracturas de los 3/5 mediales usan clavo intramedular de Küntscher. Es la indicación de elección en las fracturas de 1/3 medio de la diáfisis, aun cuando los especialistas no han logrado ponerse de acuerdo acerca de cuál de los dos procedimientos (placa o clavo endomedular) ofrece una mayor garantía de estabilidad al foco y permite una más rápida rehabilitación física.
En general las complicaciones que amenazan a esta cirugía constituyen un desastre de proporciones incalculables: osteomielitis masiva del fémur, necrosis diafisiaria, pseudoartrosis, re-operaciones, período de años de recuperación, atrofias musculares invencibles, rigideces articulares invalidantes, son sólo una parte de la formidable lista de complicaciones que siguen a la cirugía de la fractura de la diáfisis femoral, realizada en condiciones inadecuadas.
- Enfermo estabilizado y en condiciones de soportar un acto quirúrgico de gran envergadura.
- Cirujano y equipo quirúrgico de reconocida solvencia y experiencia en cirugía ósea.
- Infraestructura hospitalaria excelente, en especial en lo que se refiere a garantías de asepsia, apoyo anestésico, transfusión y radiológico.
- Dotación completa de instrumental especializado.
El peor de los resultados conseguido por un tratamiento ortopédico mal realizado, es preferible a cualquiera de las complicaciones ocurridas por una acción quirúrgica fracasada.
TRAUMA CRÁNEO-ENCEFÁLICO ABIERTO POR PROYECTIL DISPARADO POR ARMA DE FUEGO
TRAUMA CRÁNEO-ENCEFÁLICO ABIERTO
POR PROYECTIL DISPARADO POR ARMA DE FUEGO
EN PACIENTES DEL BLOQUE MÉDICO-QUIRÚRGICO,
DEL HOSPITAL ESCUELA, ATENDIDOS DESDE
MAYO DE 1998 HASTA SEPTIEMBRE DEL 2000
PENETRATING GUNSHOT-WOUND TO THE HEAD IN PATIENTS
ADMITTED AT HOSPITAL ESCUELA FROM MAY 1998
TO SEPTEMBER 2000
Meinhard Bienst-Castillo*, Lizandro Valle-Pérez**
RESUMEN.OBJETIVO.
contamos con datos propios cerca de muchas lesiones
traumáticas, eso incluye a las lesiones penetrantes de
cráneo ocasionadas por proyectiles disparados por arma
de fuego.
Por ello, decidimos iniciar un estudio preliminar de pacientes
con este tipo de lesiones para brindar una visión
general de datos de interés médico que nos sirvan para
finalmente lograr elaborar un protocolo de manejo.
De todos es ya sabido que noMATERIAL Y MÉTODOS.
de 32 pacientes con lesión penetrante de cráneo
que fueron atendidos en el Bloque Médico-Quirúrgico
del Hospital Escuela en el periodo de mayo de 1998 hasta
septiembre del 2000 (28 meses). Los datos obtenidos
directamente, ya fuera del propio paciente o sus
acompañantes o, indirectamente de los expedientes
clínicos fueron procesados con el programa Epi-Info 6.
Estudio descriptivo, transversalRESULTADOS.
fueron del sexo masculino, la media de la edad fue de
28.7 años (rango desde los 18 años hasta los 49), la mortalidad
global fue de 62.5% (20 casos). CONCLUSIÓN.
La mayoría de los datos encontrados semejan los de las
referencias consultadas, la mortalidad fue muy alta en
comparación con otras series. No hay protocolo de manejo
para este tipo de lesiones en el Hospital Escuela.
El 91% (29 casos) de los pacientesPALABRAS CLAVE:
de Glasgow, Trauma cráneo-encefálico.
Heridas por bala, Escala de ComaABSTRACT. OBJECTIVE.
It's knawn by everybodythat we doríí
injuries, and that
have our own data concerning many traumaticincludes penetrating gunshotwounds to the head.
That's why, we decided to hegin a study of a cases with
this type of
ing medical facts that at the end
a pro toco/ ofmanagement.
injury in order to have an overview of interés]will serve to elabórateMETHODS AND MATERIALS.
study of 32 patients with penetrating gimshotwound
to the head admited at the
from may 1998 until september 2000 (28 monthsj.
Al! the data gathered, either talking to the patients or
the people with him or,
processed with
RESULTS.
28.7 years oíd (range 18- 49), overall mortality was
62.5% (20 cases).
CONCLUSIÓN. Mosi ofthe residís obtainedwere similar
to the majority of references consulted, overall mortality
was high ifcompaired to other similar studies. There is no
protoco/ ofmanagement at our institution for this type of
injuries.
Descriptive, transversalSurgical Unit of Hospital Escuelathrough medical records wasEpi-Info 6.29 cases (91%) were male, median age was*
Residente de IV Año Postgrado de Neurocirugía, Universidad Nacional Autónoma de Honduras. **Departamento de Neurocirugía, Hospital escuela, Tegudgalpa, Honduras.
119
Rev Med Post UNAH Voí 5 No 2 Mayo-Agosto, 2000
DISPARADO POR ARMA DE FUEGO...
TRAUMA CRANEO-ENCEFALICO ABIERTO POR PROYECTILKEY WORDS: Gunshoí
Mead Trauma.
Wounds, Glasgow Coma Scale,INTRODUCCIÓN.
En Estados Unidos de Norteamérica, según datos
publicados en 1994, se registran aproximadamente
150 000 personas al año con lesiones ocasionadas
por bala y de estas mas de 30 000 mueren (lo cual
representa un 20%) (1); en Honduras basta leer los
diarios nacionales para darnos cuenta de la gran
cantidad de personas lesionadas por proyectiles disparados
por arma de fuego.
La mayoría de las lesiones penetrantes de cráneo se
deben en Estados Unidos de Norteamérica a misiles
(proyectiles) disparados por armas de fuego de uso
civil (1), en Honduras la mayoría de las lesiones
penetrantes cráneo-encefálicas se deben al machete
(mecanismo contuso cortante por arma blanca).
Revisando los artículos aparecidos a lo largo de
toda la historia de la Revista Médica Hondurea no
fuimos capaces de encontrar trabajos acerca de este
tema en particular, a pesar de que si aparecen trabajos
respecto al trauma cráneo-encefálico en general;
inclusive en uno de ellos hay mención del arma
blanca como uno de los agentes etiológicos principales
(2).
La morbi-mortalidad de las lesiones en estudio es
alta (3-6) su manejo médico es complejo y existe
controversia acerca de que pacientes operar y cuales
no.
Si bien es cierto que este tipo de lesiones en particular
no ha sido muy frecuente en el pasado debemos
tener en cuenta que si lo son las lesiones ocasionadas
por bala en forma general, y precisamente es
por ello que actualmente se piensa en legislar por
mayores restricciones para tener acceso a las armas
de fuego.
A medida que aumenten las lesiones ocasionadas
por bala en forma general también es lógico suponer
que deban aumentar las que involucren el cráneo.
Grahm et al. (3) proponen un protocolo de tratamiento
basado en hallazgos clinicos y tomográficos,
Taha et al. (4) amplían este protocolo, en los cuales
inclusive pacientes con puntajes muy bajos en la
Escala de Coma de Glasgow son candidatos a cirugía
tomando siempre en cuenta los hallazgos de
imagen y otras características clínicas.
A pesar de la existencia de múltiples estudios acerca
del manejo de pacientes con lesiones penetrantes
de cráneo por proyectil disparado por arma de fuego
aún existe mucha controversia acerca de la extensión
del procedimiento quirúrgico y quien debe ser
operado y quien no (7).
En este estudio se describen las características clínicas
de 32 pacientes de 18 o mas años de edad con
diagnóstico de trauma penetrante cráneo-encefálico
ocasionado por proyectil disparado por arma de
fuego y la evolución de los mismos ya sea que se
hayan operado o no.
MATERIAL Y MÉTODOS.
Estudio descriptivo, transversal de 32 pacientes, de
18 o mas años de edad, atendidos en el Bloque Médico-
Quirúrgico del Hospital Escuela, atendidos
desde el primero de mayo de 1998 hasta el treinta
de septiembre del 2000 (28 meses), todos ellos con
diagnóstico único o al menos principal de trauma
penetrante cráneo-encefálico ocasionado por proyectil
disparado por arma de fuego. Se atendieron
55 pacientes en el período del estudio, pero esta
muestra fue de 32 pacientes ya que 23 pacientes
fueron excluidos; 12 lo fueron por tener menos de
18 años de edad, 9 pacientes se excluyeron por
llegar ya muertos a la emergencia y 2 de los 23
pacientes fueron excluidos porque fueron trasladados
luego a otra institución y se perdieron al seguimiento.
En los casos de pacientes menores de edad (menor
de 21 años) se tuvo que conseguir la autorización
por escrito de los padres (o del adulto a cargo) para
ser intervenido quirúrgicamente en caso de haberse
decidido la cirugía. Si no había al momento del ingreso
del paciente ninguna persona responsable del
mismo y el estado del paciente era crítico y la cirugía
mandatoria se operaba aún sin consentimiento
escrito, Si la condición clínica del paciente menor
de edad permitía un compás de espera seguro antes
de la cirugia se difería la misma hasta contar con la
autorización quirúrgica por escrito. En los casos de
mayores de edad, si estos o en su defecto (por no
poder el paciente) su familia no autorizaban la
cirugía esta no se llevaba a cabo aunque el médico
tratante lo considerase pertinente. En vista de que los
pacientes de este estudio no fueron ingresados y
tratados en su totalidad por los autores sino que
en muchas de las ocasiones por
120
Rev Med Post UNAH Vol 5 No. 2 Mayo-Agosto, 2000 TRAUMA CRANEO-ENCEFALICO ABIERTO POR PROYECTIL
DISPARADO POR ARMA DE FUEGO...
alguno de los otros 8 residentes de neurocirugía del
mencionado hospital en muchas de las ocasiones las
variables que se pretendían investigar no fueron
consignadas, los manejos médicos difirieron según
el residente tratante y en ocasiones un mismo residente
daba manejos médicos diferentes, todo ello
producto de no existir en el Hospital Escuela un
protocolo de atención para este tipo de lesiones. Si
bien el manejo médico varió de residente a residente
e inclusive de paciente a paciente, no fue así
con el manejo quirúrgico en los casos en que el paciente
era llevado a sala de operaciones. El manejo
operatorio de estas lesiones fue el mismo en
términos generales y consistió en limpieza quirúrgica,
debridamiento, esquirlectomia, evacuación
de hematomas y cuerpo extraños mediante irrigación
exhaustiva con solución salina normal según
accesibilidad a los mismos y durorrafia ya fuese
primaria o con injertos.
A ningún paciente se le colocó monitores de presión
intracraneana tal y como se postula en otros centros
(l
hospital del estudio.
La información se recolectó mediante un cuestionario
previamente elaborado para tal fin. Todo el
análisis estadístico se hizo gracias al programa Epi-
Info 6 (Versión 6.04 b, enero 1997. Cen-ters for
Disease Control & Prevention [CDC] U.S.A.
World Health Organization, Geneva, Swit-zerland).
RESULTADOS.
Se recolectaron 32 casos en los 28 meses que duró
el estudio (1.14 casos por mes), de estos 91% fueron
hombres y
28.7 años con un rango de 18 hasta los 49 años. En
el 71% de los pacientes sus edades van desde los
18 hasta los 34 años, el 50% de los pacientes
recibió atención antes de su llegada al Hospital Escuela.
De los 23 pacientes a los cuales se les consignó el
lugar en que sufrieron el trauma, 16 (70%) de ellos
lo sufrieron en el departamento de Francisco Morazán.
La media del tiempo transcurrido entre la lesión y la
atención del paciente (fuera del Hospital Escuela)
fue de 54 minutos, entre la lesión y su llegada al
Hospital Escuela fue de 263 minutos (mas de 4
horas), entre la lesión y la cirugía fue de 1230.8
minutos (mas de 20 horas), entre la llegada del paciente
al Hospital Escuela y la cirugía fue de 828.1
minutos (más de 13 horas).
Al 59% (19 casos) de los pacientes se les hizo estudios
de radiología simple en el Hospital Escuela o
ya las traían de la unidad prestadora de servicios
que los refirió. El hallazgo mas frecuente (19 veces)
de los estudios de radiología simple fue la fractura,
le sigue la presencia del proyectil y/o las esquirlas
(15 veces).
Sólo al 40.63% de los pacientes se les hizo tomografía
axial computada cerebral, en algunos casos
porque el paciente falleció rápidamente y en otros
porque el médico tratante no la indicó. En 12 de las
13 tomografías cerebrales hechas se evidenció
fractura, en 9 de los estudios hechos se evidencia
neumoencéfalo.
El 40.6% de los pacientes tienen un puntaje en la
escala de coma de Glasgow al ingreso entre 3 y 5
inclusive, 15.6% de los pacientes tienen un puntaje
en la escala de coma de Glasgow entre 6 y 8 inclusive;
lo anterior muestra claramente que el 56.2%
de los pacientes tienen un puntaje en la escala de
coma de Glasgow que los clasifica como pacientes
con trauma severo.
Llama poderosamente la atención que al 12.5% de
los pacientes no se les consigna en el expediente al
momento del ingreso a la emergencia el puntaje en
la escala de coma de Glasgow, siendo este dato de
suma importancia como variable para toma de decisiones
terapéuticas, pronóstico y como parte integral
y primordial de todo examen neurológico (Ver
Cuadro 1).
A26 pacientes (81%) no se les solicitó cupo en la
f 5-10) ya que no se cuenta con los mismos en el9% mujeres, la media de edad fue de121
Rev Med Post UNAH Vol 5 No. 2 Mayo-Agosto, 2000 TRAUMA CRANEO-ENCEFALICO ABIERTO POR PROYECTIL
DISPARADO POR ARMA DE FUEGO...
unidad de cuidados intensivos; sólo a 1 de los 6 pacientes
a los cuales se les solicitó el cupo se le dio.
La mortalidad global fue de 62.5% (20 casos). Sólo
a 6 (50%) de los 12 pacientes que sobrevivieron se
les consignó la escala de coma de Glasgow al egreso.
A ningún paciente se le consignó la escala de
resultados de Glasgow al egreso. De los 32 pacientes
del estudio sólo 4 (12.5%) egresan con 15 puntos en
la escala de coma de Glasgow; en relación a los
pacientes que sobrevivieron (12 casos) esto
representa 33% (Ver cuadro 2). La mortalidad
quirúrgica fue de 39%, esto obedece a que de los 32
pacientes del estudio sólo se operó a 18 de ellos y
de esos 18, fallecieron a pesar de la cirugía 7.
13 pacientes del grupo de no operados (14 casos)
fallecieron, sólo sobrevive un paciente de los 14
pacientes del subgrupo de pacientes que no fueron
intervenidos quirurugicamente. Lo anterior arroja
una mortalidad de 93% para el subgrupo de pacientes
no intervenidos quirúrgicamente. Es
extremadamente importante recalcar que en el
subgrupo de pacientes no intervenidos quirúrgicamente
se dan los puntajes mas bajos en la escala de
coma de Glasgow al ingreso.
De los 20 pacientes que fallecieron durante el estudio
observamos un dato muy interesante, 70% de
ellos (14 pacientes) al ingreso tienen un puntaje en
la escala de coma de Glasgow igual o menor a 8
puntos, lo cual los clasifica como pacientes con
trauma severo: además se arroja el siguiente dato,
60% de los casos (12 pacientes) tienen un puntaje
en la escala de coma de Glasgow al ingreso de cinco
o menos, lo cual los clasifica en el subgrupo de
pacientes con peor pronóstico según los protocolos
mas aceptados de manejo (Ver cuadro 3).
El 33% de los pacientes que sobrevivieron tienen al
ingreso 8 o menos puntos en la escala de coma de
Glasgow, o sea que sólo 33% son pacientes catalogados
como pacientes con trauma severo. Sólo
8.3% de los casos (1 paciente) tienen al ingreso un
122
Rev Med Post UNAH Vol 5 No 2 Mayo-Agosto. 2000 TRAUMA CRANEO-ENCEFAUCO ABIERTO POR PROYECTIL
DISPARADO POR ARMA DE FUEGO...
puntaje en la escala de coma de Glasgow de cinco o
menos puntos (Ver cuadro 4).
DISCUSIÓN
En esta serie el 91% de los pacientes fueron hombres
y el 9% mujeres, en la serie de Grahm (9) 84%
fueron hombres y 16% mujeres; en la serie de Kordestani
88% fueron hombres y 12% mujeres y finalmente
en la revisión de Stone (5) el 90% de su
población fueron hombres y el 10% mujeres. En
cuanto a la edad, en el presente estudio hallamos una
media de 28.7; años con un 71% de la población
comprendido en el rango de los 18 a los 34 años
inclusive. En el estudio de Kordestani (9) el 75.8%
de los pacientes eran menores de 30 años. Nuestro
rango de edad fue de los 18 a los 49 años inclusive,
ese mismo rango se dio en la serie de Salzano (4).
En este estudio sólo el 50% de los pacientes recibieron
atención de personal médico y/o paramédico
previo a su llegada a nuestra institución, en la serie
de Grahm (8) ese porcentaje fue de 100%, también
fue de 100% en la serie de Levy (7), sólo en la serie
de Stone (5) se describen pacientes que llegaron en
autos particulares o caminando a la emergencia. En
esta casuística la media del tiempo transcurrido
entre la lesión y la atención del paciente (fuera de
nuestra institución) fue de 54 minutos, en la serie
de Stone (5) fue de 5.4 minutos; el mismo autor reporta
30 minutos como media del tiempo requerido
para transportar al paciente hasta el hospital en el
cual él llevó a cabo el estudio, en nuestra serie esa
misma medida fue de 263 minutos, en la serie de
Grahm (8) fue de 23 minutos, en uno de los casos de
Levy (7) ese tiempo fue de 0 minutos (al paciente le
dispararon dentro del hospital). Lo anterior creemos
obedece a la diferencia que existe en la cantidad y
calidad de los servicios de emergencia médica
(véase paramédicos) en los Estados Unidos de
Norteamérica y los de Honduras; en el país del
presente estudio básicamente se cuenta con los
servicios de la Cruz Roja, Cruz Verde, Cuerpo de
Bomberos y unos cuantos servicios privados
mientras que en países mas desarrollados, como por
ejemplo los Estados Unidos de Norteamérica con
sólo marcar por teléfono el 911 el paciente es
rápidamente atendido por una vasta red de paramédicos
que inclusive cuentan con el apoyo de
helicópteros para trasladar rápidamente a los pacientes.
Grahm (8) reporta en su serie 66% de sus pacientes
con un puntaje en la escala de coma de Glasgow al
ingreso entre 3 y 8, en nuestra serie ese porcentaje
es de 56.2%, Kordestani (9) reporta una media de 8
puntos y el 54.5% de sus pacientes tienen un puntaje
igual o menor a 8.
En este estudio la mortalidad global fue de 62.5%
(20 pacientes, n=32), y la mortalidad operatoria fue
de 39% (7 pacientes); las mortalidades en la serie
de Grahm (8) fueron de 59% y 23% respectivamente,
en la serie de Dosoglu (3) fueron de 38% y 27%
respectivamente, fue de 28% la mortalidad global
en la serie de Levy (10).
Observamos que según la fuente consultada vemos
que nuestros datos se acercan a los de algunos autores
pero difieren de los de otros, esto en parte obedece
a diferencias probablemente de nuestro sistema
de servicios médicos de emergencia (paramédicos,
véase Cruz Roja, Cruz Verde, etc) y debe ver
asimismo con el hecho de que no contamos en el
Hospital Escuela con un protocolo de tratamiento
para este tipo de lesiones.
Por ejemplo, todos los autores están de acuerdo con
el uso de fenitoina en este tipo de lesiones pero en
nuestra serie su uso no fue de un 100%; vemos
también diferencias en el uso de antibióticos, manitol,
furosemida, antitoxina tetánica y otras sustancias;
y lo mas importante en cuanto a la decisión de
operar o no.
La revisión de expedientes nos permitió observar
que diferentes residentes daban diferentes tratamientos
y en ocasiones un mismo residente daba
diferente manejo a pacientes con características similares,
esto recalco obedece a la falta de unificación
de criterios entre los diferentes médicos tratantes
y esto a su vez hace difícil la comparación de
datos principalmente en cuanto a pronóstico se refiere.
BIBLIOGRAFÍA.
1.
Trauma. En: AANS Publications Committee, Loftus
CM, editor. Neurosurgical Emergencies, Volume I.
USA: American Association of Neurologicai Surgeons;
1994. p. 59-71.
2. Lefkotea T, Trauma craneo-encefalico en el Hospital
Escuela en el periodo comprendido de agosto de
1981 a diciembre de 1983 [disertación]. Tegucigalpa
Rosenberg WS, Harsh GR. Penetrating Cerebral123
Rev Med Post UNAH Vol. 5 No 2 Mayo-Agosto, 2000 TRAUMA CRANEO-ENCEFALICO ABIERTO POR PROYECTIL
DISPARADO POR ARMA DE FUEGO...
(Honduras): Universidad Nacional Autónoma de
Honduras; 19S4.
Dosoglu M, Orakdogen M, Somay H
I. Civilian gunshot wounds to the head. Neurochirurgie
1999 Sep; 45 (3): 201-207.
Salzano A, De Rosa A, Scialpi M, Rossi E, Carbone
M, Bruñese L, et al. Ferite da arma da fuoco del cranio
osservate con Tomografia Computerizzata. Esperienza
persónate in 23 casi. [Gunshot wounds of
íhe cranium studied with computerized tomography.
Personal experience in 23 cases]. Radio! Med 2000
Jan-Feb; 99 (1-2): 26-30.
Stone JL, Lichtor T, Fitzgerald LF. Gunshot
Wounds to the Head in Civilian Practice. Neurosurgery
1995 December; 37 (6): 1104-1110.
Valadka AB, Gopinath SP, Mizuiani Y, Chacko AG,
Robertson CS. Similarities between civilian gunshot
wounds to the head and nongunshot head injuries. J
Trauma 2000 Feb; 48 (2): 296-302.
Levy ML, Masri LS, Lavine S, Apuzzo MLJ. Outcome
Prediction after Penetrating Cramocerebral Injury
in a Civilian Population: Aggressive Surgical
Management in Patients with Admission Glasgow
Coma Scale Scores of 3, 4, or 5. Neurosurgery 1994
July; 35(1): 77-90.
8. Grahm TW, Williams FC, Harrington T, Spetzler
RF. Civilian Gunshot Wounds to the Head: A Prospective
Study. Neurosurgery 1990; 27 (5): 696-700.
9. Kordestani RK, Counelis GJ, McBride DQ, Martin
NA. Cerebral Arterial Spasm after Penetrating Craniocerebral
Gunshot Wounds: Transcranial Doppler
and Cerebral Blood Flow Fíndings. Neurosurgery
1997August;41 (2): 351-353.
10. Levy ML, Rezai A, Masri LS, Litofsky SN, Giannotta
SL, Apuzzo MLJ, et al. The Significance of
Subarachnoid Hemorrhage after Penetrating Craniocerebral
Injury: Correlations with Angiography and
Outcome in a Civilian Population. Neurosurgery
1993 April; 32 (4): 532-542; Ates O, Ziyal
Suscribirse a:
Entradas (Atom)



